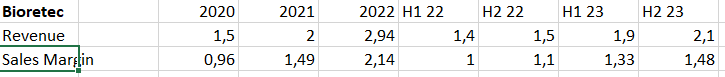Timo Lehtonen, Bioretec Oy:n toimitusjohtaja:
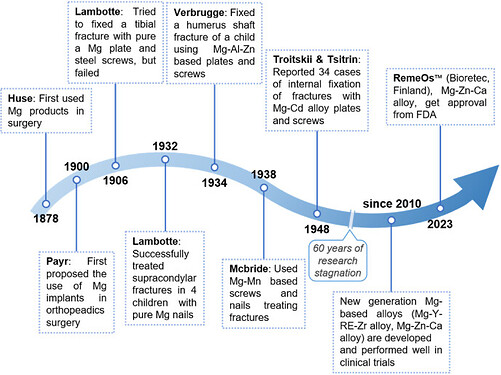
”Vuonna 2023 Bioretec saavutti historiallisen virstanpylvään, kun RemeOsTM-magnesiumseosruuvimme sai ensimmäisenä maailmassa Yhdysvaltain elintarvike- ja lääkeviranomaisen FDA:n myyntiluvan biohajoavalle metallituotteelle. Tämä merkittävä saavutus ei pelkästään avaa ovea maailman suurimmalle ortopediselle markkinalle vaan myös luo vahvan perustan koko innovatiivisen RemeOsTM-tuotelinjamme kaupallistamiselle. Jatkuvien, biohajoaviin ortopedisiin ratkaisuihin keskittyvien panostustemme seurauksena vuoden 2023 liikevaihto päätyi Bioretecin historian korkeimpaan.
Myyntiluvan saamisen jälkeen aloitimme mahdollisten eri jakelukanavien huolellisen arvioinnin, jonka jälkeen valitsimme yhteistyökumppaniksemme Spartan Medicalin. Tämä yhteistyö on strategisesti merkittävä, koska Spartanilla on laaja verkosto ja kokemus sekä siviilipuolen että Yhdysvaltain puolustusministeriön ja veteraanien terveydenhoidon (DoD ja VA) markkinoista. Jakelusopimuksen solmimisen jälkeen käynnistimme sairaalahyväksyntäprosessit ja RemeOs™-tuotteidemme lanseerauksen valituissa Yhdysvaltain huipputason akateemisissa keskuksissa ja sairaaloissa. Koska nämä prosessit ovat aikaa vieviä, odotamme parhaillaan hyväksyntöjä valituilta akateemisilta keskuksilta ja sairaaloilta. RemeOsTM-magnesiumruuvin toimitukset Spartanille alkoivat vuoden 2023 viimeisellä neljänneksellä, ja ensimmäinen leikkaus RemeOs™-ruuveilla on suoritettu.
Vahvistimme viime keväänä merkittävästi taloudellista asemaamme menestyksekkään rahoituskierroksen myötä. Vaikka rahoitusmarkkinoiden olosuhteet olivat haastavat, onnistuimme keräämään 10 miljoonan euron bruttovarat institutionaalisille ja muille kokeneille sijoittajille suunnatulla osakeannilla. Tämä lisäpääoma on erittäin tärkeä yhtiöllemme, koska sen avulla pystymme nopeuttamaan RemeOsTM-tuotelinjamme kaupallistamista ja jakelun aloittamista. Lisäksi näitä varoja käytetään tuotekehitysprojektiemme edistämiseen ja tuotantokapasiteettimme laajentamiseen, mikä asettaa meidät hyvään tilanteeseen tulevaa kasvua varten. Rahoituskierroksen jälkeen päätimme siksi investoida uuteen tällä hetkellä vain RemeOs™-ruuveillemme tarkoitettuun CNC-työstökeskukseen, jonka käyttöönotto saatiin valmiiksi tammikuussa 2024. Tukeaksemme kasvavia toimintojamme olemme ryhtyneet laajentamaan tuotantotilaamme. Lisäksi investoimme uuteen ERP-järjestelmään, jonka käyttöönotto on suunniteltu vuodelle 2024. Tämä järjestelmä on suunniteltu tehostamaan toimintojamme, ja se mahdollistaa vuoden 2023 saavutuksemme ylittämisen, jolloin toimitimme tuotteita yli 35 tuhanteen kirurgiseen toimenpiteeseen. Näiden toimenpiteiden rinnalla nopeutamme myös tuotekehitystämme kasvattamalla organisaatiotamme ja jatkamme innovointia vastataksemme markkinoiden kehittyvään kysyntään.
Vuonna 2023 liikevaihtomme kasvoi 33 prosenttia edellisvuodesta 3,9 miljoonaan euroon. Kasvuun vaikutti merkittävästi uusi RemeOsTM-ruuvimme, jonka myynti Yhdysvalloissa oli tuotteen markkinoilla olon ensimmäisen kuuden kuukauden aikana 374 tuhatta euroa. Activa-tuoteryhmän myynti oli 3,5 miljoonaa euroa, josta suurin osa, yli 50 %, tuli edelleen Kiinasta. RemeOsTM- ja Activa-tuotteiden myynti kehittyi hyvin Yhdysvalloissa, mistä kertyi lähes 22 % vuoden kokonaisliikevaihdosta. Euroopassa kohtasimme useita haasteita. Toimintaamme siellä vaikutti huomattavasti toimitusten lopettaminen Venäjälle. Lisäksi pandemian jälkiseurausten vaikutus yhdistettynä vallitsevaan akuuttiin sairaalahenkilökunnan pulaan verotti myyntiämme tällä markkina-alueella.
Vuoden 2024 ensimmäisen neljänneksen aikana arvioimme viimein saavamme RemeOs™-traumaruuvillemme myyntiluvan Euroopassa. Viivästykset ovat johtuneet Ilmoitetun laitoksen (Notified Body) pitkittyneestä hyväksymisprosessista. CE-merkin saaminen avaa tien tuotteen kaupallistamiselle Euroopan markkinoilla. Samanaikaisesti jatkamme RemeOs™-ruuvien lanseerausta Yhdysvaltain markkinoilla ja investoimme merkittävästi uusien RemeOs™-tuotteiden kehitykseen. Osana laajentumissuunnitelmiamme valmistelemme myös RemeOs™-ruuvien seuraavaa Yhdysvaltojen myyntilupahakemusta, ja olemme tehneet sopimuksen kliinisen tutkimuksen suorittamisesta RemeOs™ DrillPinille Grazin lääketieteellisessä yliopistosairaalassa Itävallassa. Tämä on tärkeä askel kohti tavoitettamme kaupallistaa DrillPin vuonna 2025.
Vuoden 2024 ensimmäisen puoliskon aikana tuotannon keskeytykset, jotka johtuvat muun muassa uuden CNC-työstökeskuksemme käyttöönotosta ja validoinneista, tulevat osittain rasittamaan toimintaamme. Tästä syystä arvioimme suuremman osan liikevaihdostamme kertyvän toisen vuosipuoliskon aikana. Koska RemeOs™-tuotelinjamme on pääasiassa kehitys- ja kaupallistamisvaiheessa, jatkamme merkittäviä investointeja sekä myynti- ja markkinointi- että tutkimus- ja tuotekehitystoiminnassamme tänä vuonna. Bioretecin uuden toimitusjohtajan rekrytointiprosessi on parhaillaan käynnissä, ja olen siirtymässä toiseen johtotehtävään organisaatiossamme. Olen tyytyväinen voidessani keskittyä jatkossa RemeOs™-tuotelinjan tulevien tarpeiden toteuttamiseen. Olen varma, että yhdessä uuden toimitusjohtajan kanssa kasvamme entistä vahvemmin uudistamaan luunmurtumien hoitoa ja parantamaan merkittävästi potilaiden elämänlaatua.”
Komee vuosi tulossa  Ihan turha kasvuyhtiöissä tuijottaa menneitä vaan katse vahvasti tulevaisuuteen ja se on Bioretecillä kirkas
Ihan turha kasvuyhtiöissä tuijottaa menneitä vaan katse vahvasti tulevaisuuteen ja se on Bioretecillä kirkas