Laitetaan tälle myös oma ketju pystyyn. Uusi lääke yhtiö First North-listalle duolistauksen kautta. Kiva lisä Helsingin pörssiin ![]()
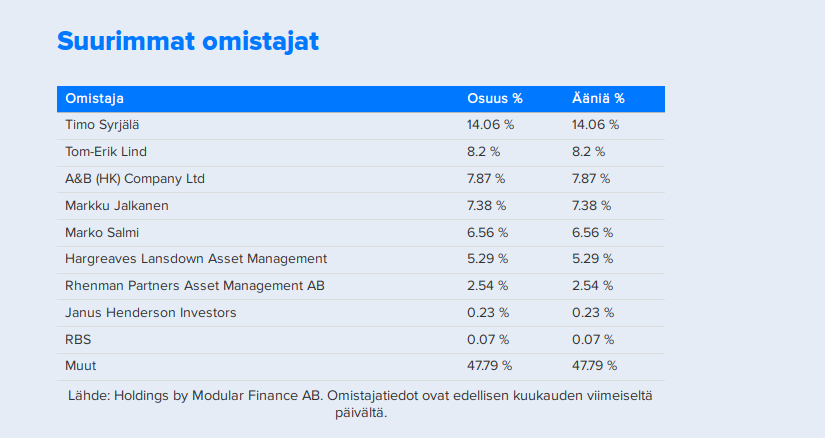
Yhtiösivulla näkyy nyt top 10 omistajat: Faron Pharmaceuticals | Inderes: Osakeanalyysit, mallisalkku, osakevertailu & aamukatsaus
Lottolappuja ![]()
Ainoastaan JNJ löytyy salkusta. Muuten mennään puhtaasti ETF:n kautta mikäli on jostain syystä pakko sijoittaa toimialaan
Mutta rohkea rokan syö (joku muu kuin allekirjoittanut)
En nyt millään halua olla taas niilo-negatiivisena, mutta kun ensin listaudutaan ulkomaille, jonka jälkeen haetaan rahoitusta rajatulta sijoittajoukolta, jonka jälkeen haetaan joukolta yksityissijoittajia ja vieläpä Suomesta niin minun nenään iskee aina hienoinen lannantuoksu ![]()
Yritetään saada toimari meille haastatteluun. ![]()
Haetaanko kuitenkaan Suomesta lisärahoitusta? Eikö tämä ole vain rinnakkaislistaus näkyvyyden ja muun sellaisen kannalta?
Rahat riittävät ensimmäiselle kvartaalille. Myyntiä kun ei ole ja kulut pyörivät niin kassa kuluu nopeaan tahtiin
Faronilla on rahoitus kunnossa seuraavaksi 12 kuukaudeksi marraskuussa toteutetun rahoituskierroksen jälkeen, mikä on myöskin edellytys First Northiin listautumiseen. Lisärahoitusta ei haettu First Northiin listautumisen yhteydessä eikä nähtävästi haetakaan lähiaikoina, koska edellisessa rahoituskierroksessa Faron sitoutui olemaan tekemättä osakeanteja vähintäänkin seuraavaan 6 kuukauteen.
Kaikki tiedot löytyvät AIM:n pörssitiedotteista. Näistä tiedotteista ilmenee myöskin, että Faron neuvottelee lisenssisopimuksista usean partnerin kanssa koskien Clevegen immuunisyöpälääkettä ja neuvottelut on tarkoitus saada päätökseen lähikuukausina. Tämän tyyliset sopimukset ovat yleensä huomattavan suuria, joten yhtiöllä on valtava potentiaali, mikäli he saavat lisenssisopimuksen/sopimukset aikaiseksi.
Kannattaa ensin tutustua yhtiöön kunnolla ennen kuin alkaa kommentoimaan. DYOR.
Oma moka. En huomannut tuota ilmoitusta, vaan sanoin vain mitä viime osarissa oltiin mainittu. Eli rahat loppumassa ja lisää tarvitaan. Hyvä kuitenki jos asia on hoidossa hetkeksi aikaa
Kehitystyö on kuitenkin kallista ja muuttuu kalliimmaksi ilman varmuutta saadaanko markkinoille mitään myytävää. Näitä firmoja ei Suomessa ole juuri ollut ja asia on varmasti uusi suurimmalle osaa palstalaisia. Riski menettää merkittävä osa pääomasta on näissä firmoissa hyvin todennäköinen ja tuskin juuri kenelläkään on asiantuntemusta arvioida saadaanko lääkettä markkinoille faasitutkimusten edetessä
Tältä kannalta rahoituspohjan laventaminen on tärkeää. Epäilystä kuitenkin itsessäni herättää, kun skipataan OMXH Helsinki ja myöhemmässä vaiheessa haetaan listausta myös tänne. Terve epäily on aina hyvästä
Eiköhän alun perin tarkoitus ollut listautua ulkomaille ja päästä maaliin asti Traumakinen kanssa, mutta kun tuo meni pääindikaatiossa Faasi 3:ssa puihin, niin nyt on tarvinnut myös muita mahdollisuuksia tutkiskella. Tämä lähinnä mutuna, mutta jos Traumakine olisi onnistunut, niin epäilen että tänne oltaisiin lähdetty rinnakkaislitautumista hakemaan.
Mitäs mieltä palstalaiset tämän päiväisestä MATINS-päivityksestä? Itse ainkain tulkitsen tämän jälleen positiiviseksi viestiksi kyseisen tutkimuksen osalta.
Huomasin tämän uutisen tänään. Tämä taitaa olla jatkoa lokakuussa ilmoitetusta tuotantopäivityksestä?
https://otp.tools.investis.com/clients/uk/faron1/rns/regulatory-story.aspx?cid=2223&newsid=1355518
Aloitin tutkimaan tätä Farnon Pharmaceuticals yhtiötä vähän enemmän. Olen toistaiseksi sijoittanut firmoihin joiden tilipäätöstiedoissa on selkeästi enemmän tuottoja kuin menoja joten tämä olisi siihen joukkoon aivan täysi vastakohta. Muutenkin kyseessä voisi olla enemmän hyväntekeväisyys kun sijoitus mutta tulisipa haastettua itseään astumaan täysin oman osaamisalueen ulkopuolelle ![]()
![]()
![]()
Löytyiskö mitään järkiperusteita tälläiseen lääkeyhtiöön sijoittamisen puolesta?
Löysin mielenkiintoisen blogin, jossa puhutaan lääkeyhtiöihin sijoittamisesta. En ehtinyt sitä vielä juuri lukea, mutta pari juttua ajattelin laittaa tänne muidenkin iloksi ![]()
Lääkärin resepti: helmikuuta 2013
Löysin Faronista myös pari videota YouTubesta joita ei ollut firman omilla sivuilla.
Hot off the press ![]()
![]()
![]()
http://otp.investis.com/clients/uk/faron/rns/regulatory-story.aspx?newsid=1358299&cid=2223
Laitoin tästä itse tänään pienen position. Potentiaalia on nousta paljon ja nopeasti. Siitä en tiedä miten järkevää on. Menee raha ainakin hyvään tarkoitukseen toivottavasti jos menee.
Vähän samoja ajatuksia täällä. Luin jostain sijoituskirjasta tai kuulin sen podcastin kautta, että sijoittamisessakaan ei kehity jos ei koskaan haasta itseään oman mukavuusalueen ulkopuolelle. Tykkään itse perehtyä asioihin joten jos laittaa tähän vähän rahaa kiinni samalla “hyväntekeväisyys” periaatteella niin tuleepahan ainakin opiskeltua taas jotain itselle tuntematonta.
Faronilla on aktiivinen kannattajaryhmä täällä. Kovasti odottavat että hyviä uutisia pitäisi alkaa tulemaan lisää.
https://m.fi.investing.com/equities/faron-pharmaceuticals-Oy tuolta katselen välillä tuota kurssia. Näkee myös että tällähetkellä on strong buy suositus.
Faron on myös uusinut nettisivunsa
Ostan pienen position huomenna niin pysyy mielenkiinto paremmin yllä.
Mitä mieltä olette Faronin uusista kotisivuista?
Pidin siitä että Pipeline osiosta näkyy nyt tosi selkeästi kaikki käynnissä olevat tutkimukset ja missä vaiheessa ne ovat.
Uusi RNS tiedote Faronilta tänään. En nähnyt sitä vielä kotisivuilla niin kopioin sen tähän. Lyhyt aika mitä olen seurannut Faronia niin RNS tiedotteet saavat aikaan säpinää ja osakekurssi menee mukavasti ylöspäin, jos uutinen on positiivinen. Jos ymmärrän oikein niin nyt lääkkeelle testataan mahd uusi kohderyhmää?
Faron Pharmaceuticals Oy
(“Faron” or the “Company”)
MATINS TRIAL UPDATE
Ovarian cancer selected as second expansion cohort
Company announcement, 27 January 2020 at 9.00 AM (EET)
Inside information
TURKU - FINLAND - Faron Pharmaceuticals Oy (AIM: FARN, First North: FARON), the clinical stage biopharmaceutical company, today announces that the second expansion cohort in its phase I/II MATINS clinical trial investigating the safety and efficacy of Clevegen will be in patients with ovarian cancer.
The ongoing phase I/II MATINS clinical trial is investigating the tolerability, safety and efficacy of Clevegen, Faron’s wholly-owned novel precision cancer immunotherapy targeting Clever-1 positive tumour associated macrophages (TAM), in selected metastatic or inoperable solid tumours.
Initiation of this second expansion cohort follows approval from the MATINS trial’s data monitoring committee earlier this month to initiate the study’s first expansion cohort in patients suffering from late-stage colorectal cancer (CRC). Ovarian cancer is a tumour type known to host a significant number of Clever-1 positive tumour associated macrophages (TAM). It presents a high unmet medical need with few available treatments for patients. Large transcript analysis of ovarian tumours indicates significant outcome differences between patients with either high or low Clever-1 expression. Patients with high Clever-1 expression have short life expectancies under current treatment options.
Dr. Markku Jalkanen, Faron’s CEO, said: “Data collected so far in the MATINS trial are highly encouraging, with Clevegen establishing itself as a potential immunotherapy capable of downregulating a range of major inhibitory immune checkpoints (PD-1, PD-L1, CTLA-4) across several cancers. Initiation of this additional expansion cohort signals our commitment to rapidly progress the development of Clevegen in patients with limited effective treatment options.”
Dr. Tyler Curiel, Professor and The Daisy M. Skinner President’s Chair in Cancer Immunology Research, UT Health San Antonio, and MATINS trial site investigator and principal investigator for USA, said: “Ovarian cancer is devastating and there remains a huge need for new treatments. Expanding the MATINS trial to include ovarian cancer patients will help us to understand this novel potential immunotherapy in a patient group where we desperately need to improve outcomes. We are very excited to join the MATINS trial and to start US recruitment.”
Existing MATINS trial sites in Europe are currently recruiting for the first expansion cohort in late-stage CRC patients and this second cohort, in a total of 10 patients with ovarian cancer, is expected to follow in the coming weeks. With good tolerability and no dose limiting toxicity signals established across all dosing levels explored in the MATINS trial to date, the dosing for this additional cohort is likely to be higher (e.g. 1 mg/kg) than for the first CRC cohort. MATINS trial sites in the US are expected to begin opening in the short term.
Primarily intended to investigate safety and tolerability, the completed Part I of the MATINS trial has already shown that Clevegen administration promoted immune activation in all of the dosed patients to date. This would potentially make Clevegen a new and effective macrophage immune checkpoint drug for cancer patients, who frequently suffer from supressed immune capacity toward tumour elimination. Previously announced data also indicate that Clevegen can down regulate a range of major inhibitory immune checkpoints, that current immuno-oncology therapies aim to suppress.
This announcement contains inside information for the purposes of Article 7 of Regulation (EU) No 596/2014 (“MAR”).
For more information please contact:
Faron Pharmaceuticals Oy
Dr Markku Jalkanen, Chief Executive Officer
Panmure Gordon (UK) Limited, Nomad and Broker
Emma Earl, Freddy Crossley (Corporate Finance)
James Stearns (Corporate Broking)
Phone: +44 207 886 2500
Sisu Partners Oy, Certified Adviser on Nasdaq First North
Juha Karttunen, Jussi Majamaa
Phone: +358 (0)40 555 4727
Consilium Strategic Communications
Mary-Jane Elliott, David Daley, Lindsey Neville
Phone: +44 (0)20 3709 5700
E-mail: faron@consilium-comms.com
About the MATINS study
The MATINS study is the first-in-human open label Phase I/II clinical trial with an adaptive design to investigate the safety and efficacy of Clevegen in selected metastatic or inoperable solid tumours. The selected tumours under investigation are cutaneous melanoma, hepatobiliary/hepatocellular, pancreatic, ovarian and colorectal cancer, all known to host a significant number of Clever-1 positive tumour associated macrophages (TAM). All together these five target groups consist of approximately 2 million annual cases worldwide. Cancer patients with high Clever-1 expression are identified with a simple blood myeloid cell staining with Clevegen (“liquid biopsy”).
Part I of the trial deals with tolerability, safety and dose escalation to optimize dosing. As the trial is an open label study, the Company expects to report findings as the dosing progresses. The cohort expansion during Part II will focus on identification of patients who show an increased number of Clever-1 positive circulating monocytes and the safety and efficacy of the treatment. Colorectal cancer and ovarian cancer have been selected as the first and second expansion cohorts in Part II. During Part III, the main focus will be on assessing the efficacy of Clevegen on study subjects who show an increased number of Clever-1 positive circulating monocytes, making the treatment precisely targeted and maximizing the chances of success for efficacy. The treatment, if successful, may ultimately be used as a standalone therapy or in combination with other immunotherapies like PD-1 inhibitors.