Onhan tosta HMA:sta pohdittu, että jos aza ei toimi, deci voi toimia tai toisinpäin. Ei kai selvää näyttöä? ”role of sequential second-line HMA following first-line HMA failure is still controversial amid inconsistent clinical evidence” Cancers | Free Full-Text | What’s Next after Hypomethylating Agents Failure in Myeloid Neoplasms? A Rational Approach
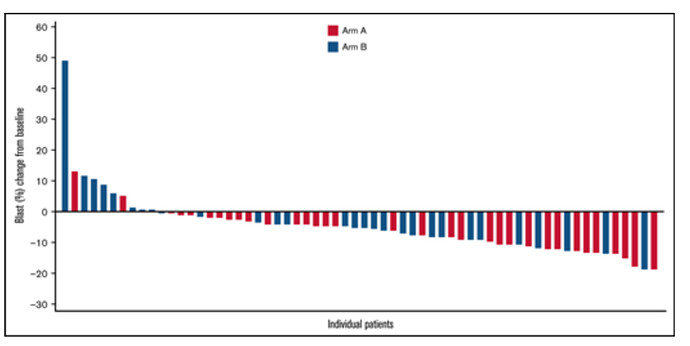
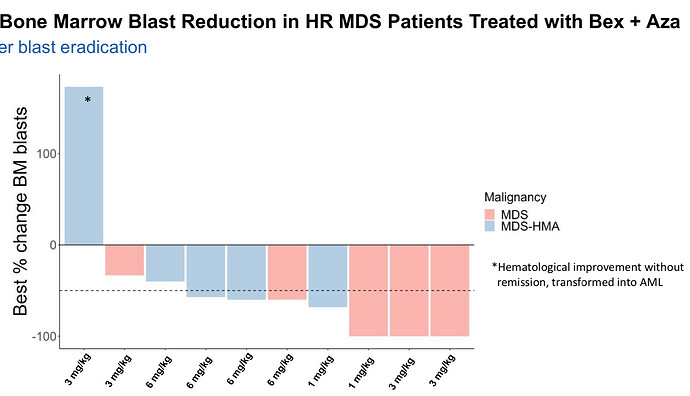
Johtuuko se mahdollinen toimiminen sitten siitä, että noiden välillä on ollut aikaa, kuten aza voi kai joskus toimia, jos edellisesta azasta on aikaa. Jos ne tulee heti perään eli on refraktaari, ei voi kai toimia, jos kerran on refraktaari  eli silloin on lähes varmasti Bexin ansiota.
eli silloin on lähes varmasti Bexin ansiota.
Yhtä kaikki. Markkukin hiukan arasteli, ainakin minun silmissäni, kun lopulta viestivät, että 100 % respondoi. Aluksi ei niin viestitty. Kyllä siellä tiedetään, mitä on todennäköisyyslaskenta ja syy-seuraussuhteet pienissä aineistoissa.Tulos on kuitenkin tulos.
Mitä pitää tehdä, kun on epävarmaa, mistä johtuu? Pitää tehdä lisää tutkimusta ja suuremmalla potilasjoukolla. No mitä tekee Faron? Faron tekee lisää tutkimusta ja suuremmalla potilasjoukolla. Faasi 2 menossa, kuten tiedetään.
Jos suuremmalla potilasjoukolla tulee loistavat vasteet, mitä tekee FDA? Saa nähdä, mahdollisesti kelpuuttaa satunnaistamattoman pivotal trialin. Tähän odotan jälleen ”ei minun mielestäni”-kommenttia. Mitä tekee FDA, jos tulokset faasi 2:ssa ovat vain tyydyttäviä? Ohjaa tekemään satunnaistetun, jota odotetaan skenessä mielenkiinnolla kontrolliryhmän suhteen. Ehkä muita trialeja r/r tapauksiin tulee, joista voi nähdä kuinka siinä ohjauksessa menetellään, onko tulossa?
Tulosten suhteen voi olla luottavainen tieteellisiin artikkeleihin, esim. Cellin MATINS, tieteellisten konferenssien posterit, ASH, EHA jne. BEXMABin tuloksista. Niitä eivät faronilaiset ole yksin laatineet. Tällä foorumilla pöyristymisen ollessa pahimmillaan, epäiltiin koko Faronia kusetukseksi, huijauksesta puhumattakaan. VerPun varpu puhdisti pahimmat pois.
Kannattaa muistaa, että huippututkijat, klinikoiden vastaavat lääkärit eivät riskeeraisi riippumattomuuttaan ja mainettaan yhden firman takia puhumalla BS:ää.