Itse ihmettelen mikäli suurin omistaja EAKR-aloitusrahasto ei osallistu osakeantiin. Omistavat kuitenkin ~19% yrityksestä, joten heidänkin etu että kierros onnistuu. Kyseisen rahaston kuitenkin tarkoitus rahoittaa tällaisia firmoja.
Maksimoidakseen muilta sijoittajilta saatavan rahan, laittavat sitten 21.8 puuttuvan pari miljoonaa pottiin?
Hei,
Tertuloa foorumille. tarkisin että teidän maili on oikea IR tilin maili, joten myönnän sille validoidun tilin ansiomerkin ![]()
FDA on myöntänyt Breakthrough Device -statuksen Injeq IQ-Tip® -älyneulalle
Injeq IQ-Tip laitteisto ja sen käyttökohteet täyttävät kriteerit ja ovat saaneet Breakthrough device -statuksen Yhdysvaltain elintarvike- ja lääkevirastolta (FDA:lta).
Injeqin toimitusjohtaja Timo Hänninen sanoo: “Olemme innoissamme tästä FDA:n tunnustuksesta. Jo yli vuosikymmenen jatkunut insinöörityö ja kliiniset tutkimukset alkavat nyt tuottaa tulosta. Ensimmäiset Injeq-tuotteet saivat eurooppalaisen myyntiluvan eli CE-hyväksynnän 2021 tiukkojen MDR-vaatimusten mukaisesti. Nyt Yhdysvaltain lääkinnällisten laitteiden viranomaiset (FDA) ilmaisevat halukkuutensa avustaa markkinoille tuloamme asiantuntija-avulla ja nopeutetulla käsittelyllä Yhdysvaltain markkinointiluvan saamiseksi.”
Tässä linkki viralliseen 14.8 julkaistuun lehdistötiedotteeseen:
Toivottavasti herättäisi jotain kiinnostusta uutismediassa, onko jokin suomalaislääke tai tuote saanut aiemmin vastaavaa luokitusta FDA:lta?
Ei ainakaan härmäläistä nimeä näkynyt listalla. Eli tuolla aiempia tapauksia ja muutenkin hyvää infoa tuosta BD-ohjelmasta.
edit. Ja näin kauan sitä väittämää kesti. Seison täällä korjattuna ja vaikka mitä. Eli Bioretec tosiaan ainakin.
Bioretecilta löytyi uutinen huhtikuulta -21, että on saanut tuon ja FDA lupa myönnetty 30.3.2023. Eli luulisi Tomi Nummisella olevan hyvin tietoa tämän kulusta.
Katsoin noita hallituksen sekä johtoryhmän kokoonpanoja ja molemmissa on tekniikan tai kauppatieteiden asiantuntijoita, mutta ei yhtään lääketieteen alalta. Heräsi kysymys, että miksi ei ole juuri tällaisella alalla?
Hallituksen jäsen Piritta Setälä ainakin on erikoislääkäri:
Lisäksi Injeqillä erillinen Advisory Board, joka muodostuu lääketieteen ammattilaisista:
Tuosta kuvakaappauksestasi klikkaat Setälän kohtaa ‘lue lisää’, niin selvästi kerrotaan:
“LT, anestesiologian ja tehohoidon erikoislääkäri, apulaisylilääkäri”
Lisäksi:
Löytyy kotisivujen kohdan ‘contact’ (english) alta.
Lisäksi samat tiedot on rahoituskierroksen sijoitusmuistiossa (vaatii kirjautumisen Invesdoriin).
Onkohan kukaan lähestynyt advisory boardia ja kysellyt, että onko tuotteella ongelmaa, jota se ratkaisee? Sijoituspäätöstä helpottaisi, jos saisi asiantuntijoilta näkemyksiä. Niiden lisäksi, jotka ovat ko. ketjussa jo kommentoineet.
Sijoitusfoorumin anonyymit nimimerkit eivät kyllä ole vielä minua vakuuttaneet siitä, ettei ratkaistavaa ongelmaa olisi ja etteikö Injeq sitä voisi ratkaista. Advisory boardista en ole kuullut.
Tutulta lääkäriltä muinoin kysyin aiheesta (perehtyi ehkä viisi minuuttia) niin totesi ettei kannata asiaa arvioida ”ison ratkaistavan ongelman” kautta. Vaan toiminnan kehittämisen kannalta ja asioiden tekeminen helpommalla. Tähänkin asti lääkärit ovat lumbaalipunktioita tehneet miljoonia ja miljoonia, mutta jos Injeq tutkitusti vähentää jälkioireita niin se on todella hieno juttu. Lisäksi jos vaan on hoitotoimenpiteiden suorittamista helpottavia innovaatioita, hoitomaailma ottaa ne mieluusti vastaan. Lääkäreistä (osaavista ja ylipäätään) tuskin on globaalia ylitarjontaa tulevaisuudessakaan.
Heikolta alkaa näyttää tämä rahankeruu kierros. Edes FDA uutiset ei saanut isompaa buustia aikaan. Olisiko kuitenkin pitänyt listautua jo puolitoistavuotta sitten kun tämä firma oli kuuminta hottia ja osakkeet olisivat menneet kuin kuumille kiville.
Nähtävästi usko mennyt sijoittajilta tahmean myynnin aloituksen vuoksi.
Saadaanko tätä listattua enää koskaan?
Itse ainakin olen alaskirjannut omat osakkeet ja vaihtovelkakirjat nollaan. Kyllä on ollut niin tahmeaa tää homma, että jos jotain saa takas niin hyvä . Ymmärrän, että se puuhamiehen kuolema varmasti vaikuttanu paljon tämän etenemiseen.
Vaikka tuo 3 milliä saataisiin, niin se ei riitä mihinkään. Itse tein se virheen, että en ei-lääkäri henkilönä tajunnut miten pieni/olematon markkina tälle on. Nuo pistokset eivät ilmeisesti ole niin suuri ongelma ja kun tämän neulan ja normi neulan hinta ero on varmaan iso. Niin ei ihme, että myynti ei vedä.
Uskon, että jos tämä saataisiin listattua niin en olisi ainoa joka laittaisi laput laitaan suoraan. Mitään sisäpiirirekisteriä ei taida olla, et saisi tietoa onko he laittamassa mitään kiinni tähän. Veikkaan, että vastaus on iso EI.
Onhan tässä semmoinen ihan mitätön mahdollisuus, että tää lähtee lentoon, mutta en pidättele hengitystä.
EDIT: Vuoden alussa vielä palkattu joku ravikuningatar kansainvälisen myynnin johtoo ei ainakaan täällä herättänyt mitään riemun kiljahduksia.
Sinun ei tarvitse spekuloida ongelman suuruutta tai neulojen hintaeroa, koska tutkimustietoa on saatavilla.
Alla artikkeli lumbaalipunktioiden onnistumisista normaalilla neulalla ja älyneulalla, ja onnistumista/komplikaatioita verrattu/suhteutettu neulojen hintaan.
Lannepiston eli lumbaalipunktion jälkeinen päänsärky (postspinaalipäänsärky) on hankala toimenpiteen jälkeinen komplikaatio, joka johtuu lannepistokanava-aukon läpi tihkuvasta selkäydinnesteestä ympäröiviin kudoksiin, jolloin selkäydinnestetilan paine laskee ja potilaan aivokalvot venyttyvät asennonmuutosten yhteydessä. Särky pahenee istumaan noustessa tai pystyasennossa, tuntuu otsalla tai silmien takana ja siihen voi liittyä pahoinvointia, ääni- tai valoyliherkkyyttä tai niskajäykkyyttä. Aivo-selkäydinnesteen vuoto saattaa aiheuttaa myös kuulo- ja näköhäiriöitä. Ilman hoitoa päänsärky voi kestää jopa pari viikkoa. Mikäli vuodelepo, nesteytys ja suun kautta otettavat särkylääkkeet eivät auta, voidaan potilaalle tehdä veripaikkaus lannepistoalueelle. Veripaikkaa varten anestesialääkäri ruiskuttaa epiduraalitilaan potilaan omaa verta. Tuolloin epiduraalitilaan muodostuva paine ja hyytymä helpottavat oireita. Lannepiston jälkeen 48 tunnin kuluessa pistetty veripaikka antaa avun jopa 90 %:lle potilaista.
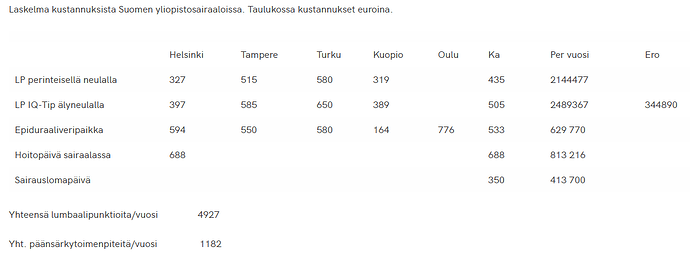
Terveyden ja hyvinvoinnin tutkimuslaitoksen vuosien 2010 – 2020 tilastojen mukaan Suomessa tehtiin keskimäärin noin 4927 lumbaalipunktiota vuodessa. Tutkimusartikkeleissa esitettyjen ilmaantuvuuslukujen perusteella arvioiden vuosittain 1182 potilasta voi saada lumbaalipunktion jälkeisen päänsäryn. Kun nämä toimenpiteet tehdään Injeq IQ-TipR laitteistolla päänsäryn esiintyvyys voi laskea jopa kuuteen prosenttiin (6 %), jolloin voimme välttää keskimäärin 886 ylimääräistä lumbaalipunktion jälkeistä päänsärkykomplikaatiota vuodessa.
Lannepistotoimenpiteen keskihinta Suomen yliopistosairaaloissa on 435 euroa. Toimenpiteen suoritus Injeq IQ-TipR laitteistolla tuo lisäkulua noin 70 euroa eli hinnaksi muodostuu 505 euroa. Veripaikkatoimenpiteen kustannus on keskimäärin 532 euroa. Yhteiskunnalle hoitopäivä sairaalassa maksaa 688 euroa ja sairauspäivä noin 350 euroa. Osa päänsärkykomplikaation saaneista potilaista tarvitsee toistetusti veripaikkatoimenpiteen tilan hoitamiseksi, ja tästäkin toimenpiteestä toipuminen vie aikaa.
Näiden lukujen perusteella lannepistot maksavat Suomessa noin 2,1 MEUR. Jos laskemme, että lannepisto Injeq IQ-TipR laitteistolla maksaa 70 euroa ja lisätään vielä tämäkin vajaa 400 000 euroa kustannuksiin, silti nykykustannukset laskevat, kun komplikaatiot vähenevät huomattavasti. Laskennallisesti pelkästään päänsärkytapaukset vähentyisivät 1182 tapauksesta 296 tapaukseen.
Tällaisessa hyvin karkeassa laskelmassa jää huomiotta potilaan kokemus. Päänsärystä pitäisi aina myös informoida toimenpiteen tehnyttä lääkäriä, mutta koska hoito voidaan tehdä eri sairaalassa, tieto ei aina tavoita häntä. Usein päänsäryn saaneet kertovat, että epämiellyttävät kivut tulivat yllätyksenä, eikä niihin edes osannut heti hakea apua. Ehkä vielä ikävämpää potilaan kannalta on se, jos lannepistotoimenpiteeseen ryhtymistä vältellään tai pitkitetään komplikaatioiden pelon takia sellaisissa tilanteissa, kun se oikeaan ja nopeaan diagnoosiin ja hoitoon pääsyn kannalta olisi ehdottoman tärkeää. Nuorille lääkäreille teknologian käyttöönotto on luontevaa, ja he ovat tottuneita hyödyntämään uusia kliinisen työn apuvälineitä. Kun käytössä on Injeq IQ-TipR laite, voi lannepiston tehdä heti jo ensiavun päivystävä lääkäri, eikä paikalle tarvitse kutsua anestesiologia. Näin voidaan lyhentää hoitoketjuja, parannetaan hoidon laatua ja säästetään aikaa sekä rahaa. Joskus myös ihmishenkiä, kun lapsen aivokalvontulehdus todetaan ajoissa.
Sairaalat kehittävät ja seuraavat jatkuvasti omia haittatapahtumarekistereitään, joiden perusteella pyritään parantamaan toiminnan turvallisuutta ja tehokkuutta. Vähentämällä komplikaatioita ja kohdentamalla oikeat hoitotoimet ja hoitomenetelmät saadaan hoitovaikuttavuus kasvamaan – siis hoidetaan potilaita paremmin ja käytetään resursseja tehokkaammin sekä yksilön että yhteiskunnan kannalta. Potilashoidon vaikuttavuus on nimetty keskeiseksi osaksi yliopistosairaaloiden strategiaa.
Pahoittelut pitkästä lainauksesta.
Oli pakko, koska tuntuu että foorumilaiset eivät jaksa tutkia asiaa (avata linkkejä) ja jokainen vuorollaan sanoo, että älyneula ei ratkaise mitään ongelmaa.
Niin tuo on firman mainospuheita. Myynnistä päätellen ketään muuta ei kiinnosta nää lannepiston mahdolliset ongelmat, kun firmaa itseään.
Nuo yllä olevat tekstit ovat firman sivulta ja tottakai tarkoitus on mainostaa laitteen etuja ja säästöjä sairaaloille mutta teksti perustuu tutkimusartikkeleihin jotka näkyvät liitteissä. Ymmärtääkseni niitä on ollut tekemässä muutkin kuin Injeqin edustajat. Eli siinä mielessä en ymmärrä tätä vähättelyä tekstiin. Mielestäni nämä mainospuheet ovat ihan asiallisa. Toinen asia sitten on miten nämä saadaan muutettua myynniksi
Injeq on myös itse tuonut kyseistä haastetta/riskiä ilmi, eikä mitenkään sitä salaile.
Kestää aikansa, että uusi teknologia otetaan käyttöön tai tekee läpimurron, varsinkin lääketieteen alalla.
Ei kai kukaan uskonut, että CE-merkinnän jälkeen voitaisiin ottaa jalka pois kaasulta ja koko maailma olisi tuotteesta heti tietoinen.
CE-merkinnästä on vasta noin 21 kuukautta.
Kunnon myynti ja markkinointi on vasta alkanut.
Nyt vain osoitetaan selkeästi, että uusi tapa on parempi kuin vanha, niin turvallisuuden kannalta kuin taloudellisesti.
On ollut ilo lukea, että parin kuukauden välein ilmoitetaan uusista jakelijoista.
Kertakäyttöisiä älyneuloja kun myydään, niin liikevaihdon kasvu voi olla suurta ja nopeaa.
Äkkirikastumista odottavat kyllä joutuvat suurella todennäköisyydellä pettymään.